戦略的研究シーズ育成事業
事業概要
戦略的研究シーズ育成事業は、地域の経済的価値(新産業・新事業)の創出や地域の社会的価値(クオリティー・オブ・ライフの向上等)の創出へ繋がる研究シーズの育成を目的とした共同研究事業です。研究課題は毎年度、公募・選考によって選出します。本事業終了後は、KISTECが実施する大型の研究事業への展開を目指していただきます。
研究課題
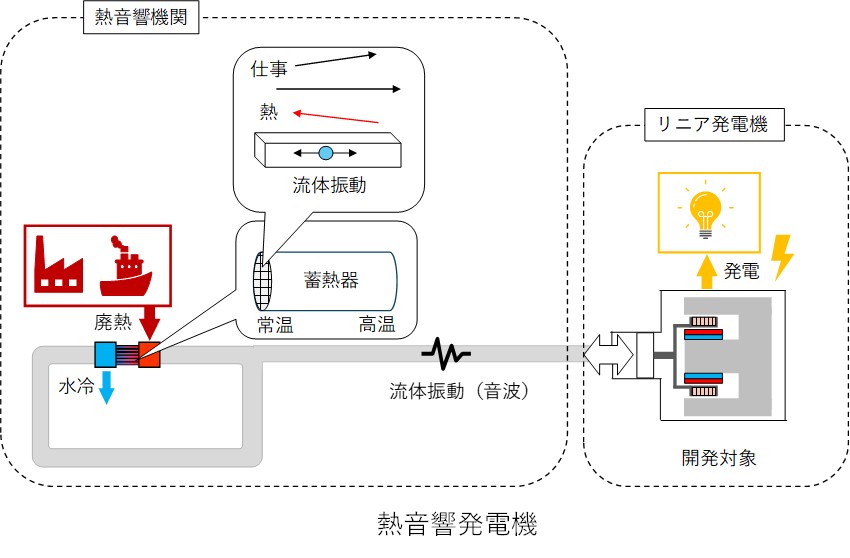
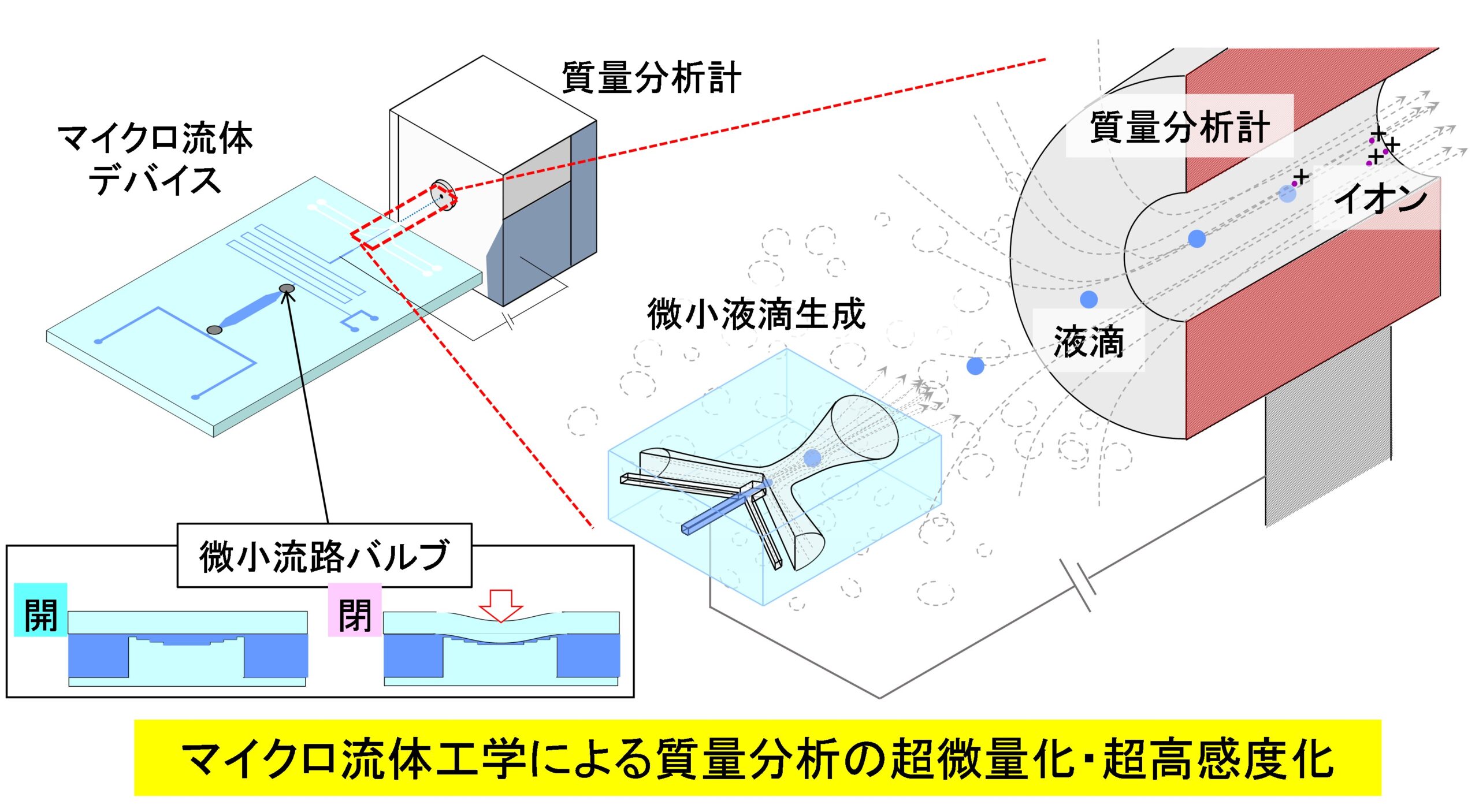
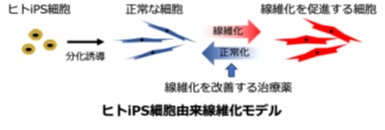
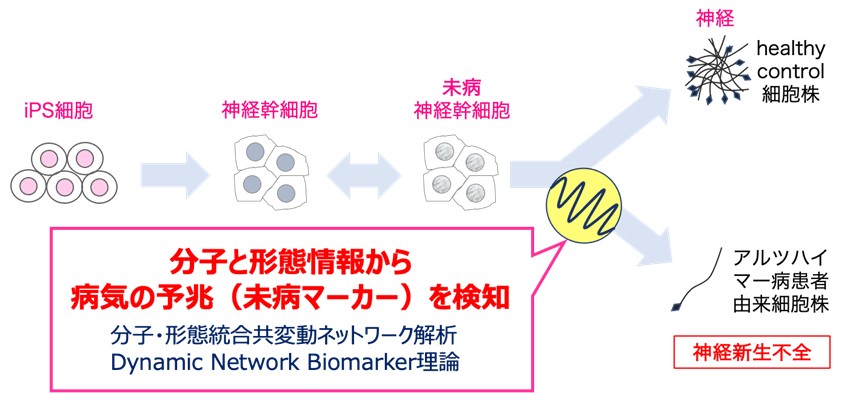
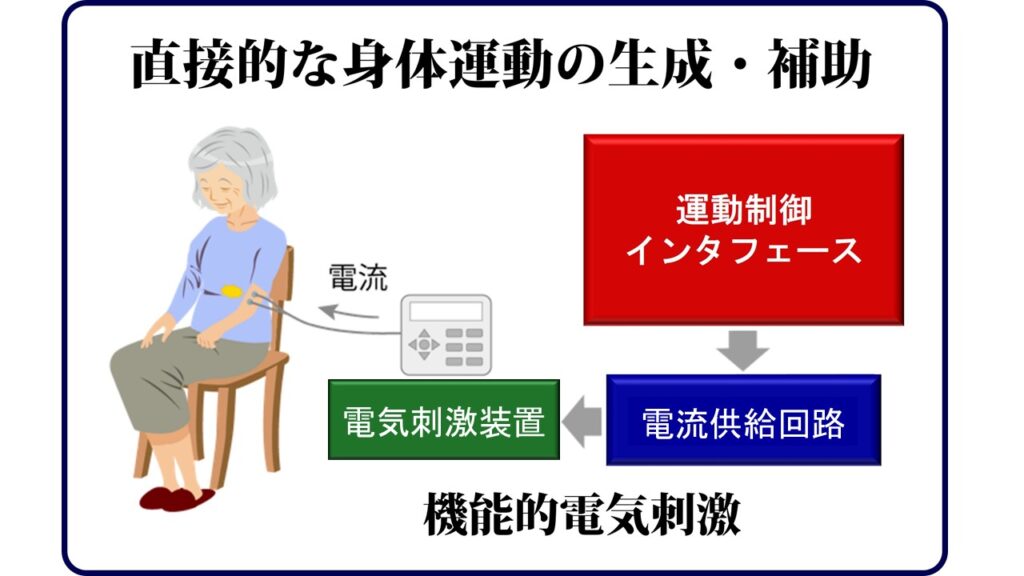
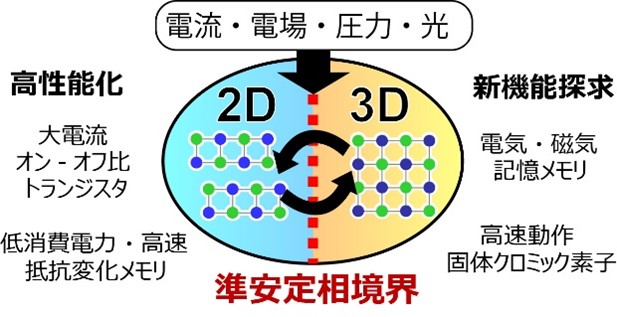
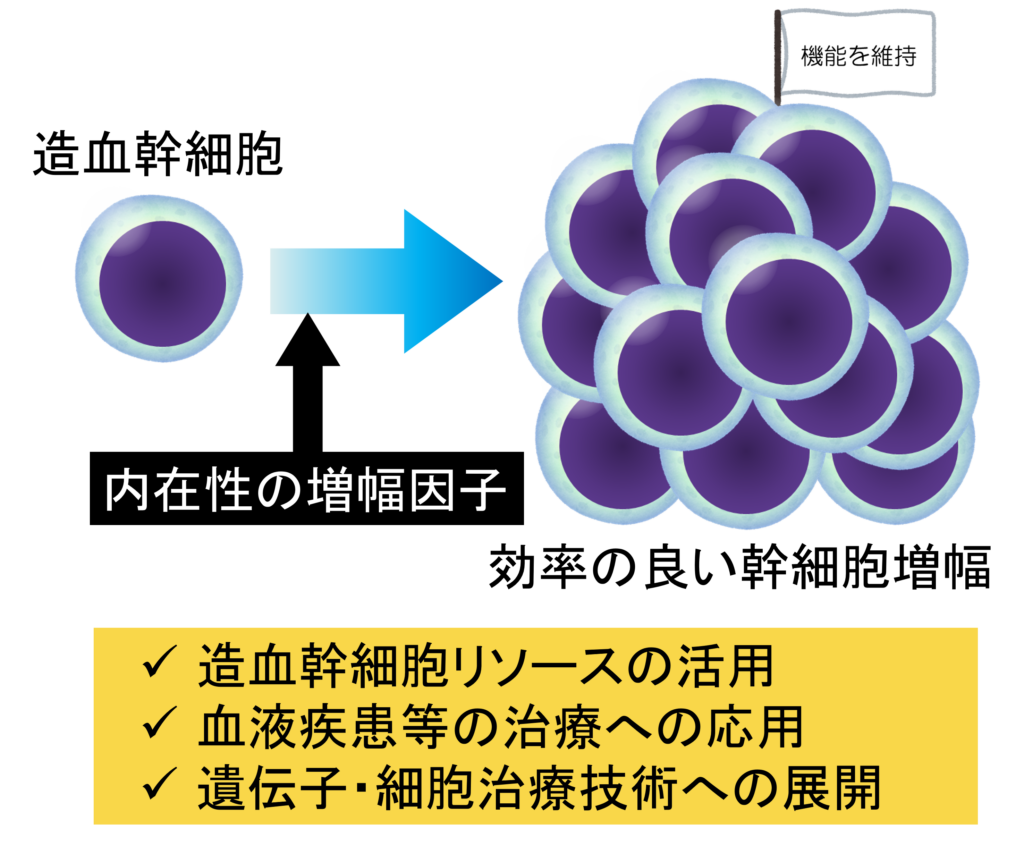
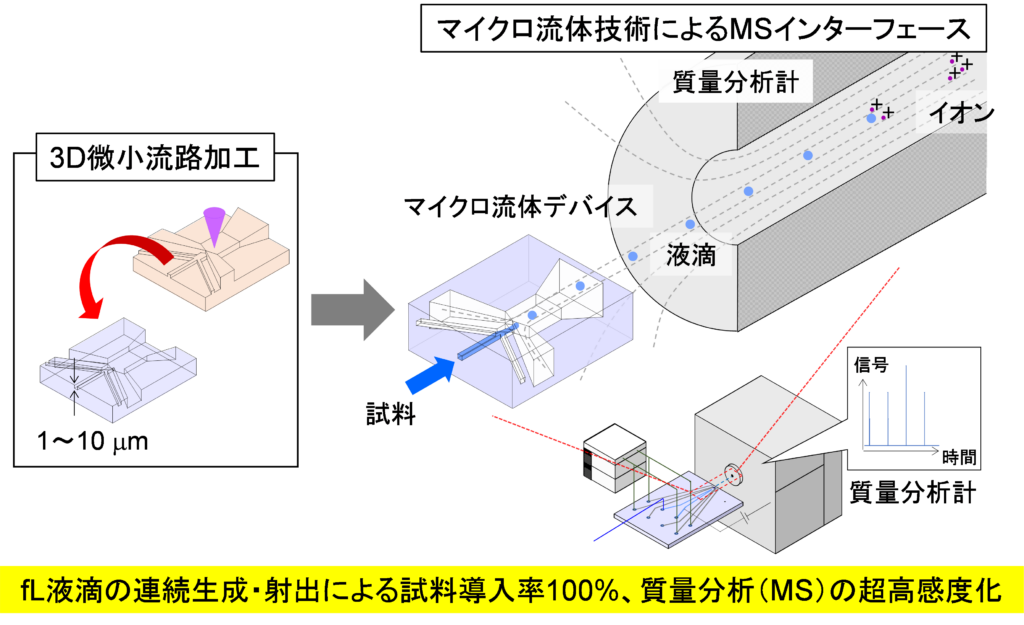
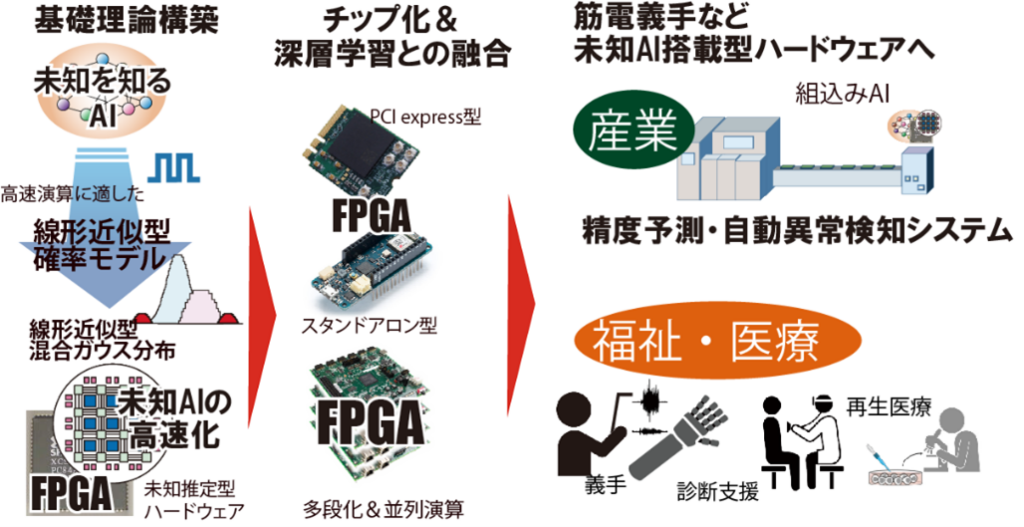
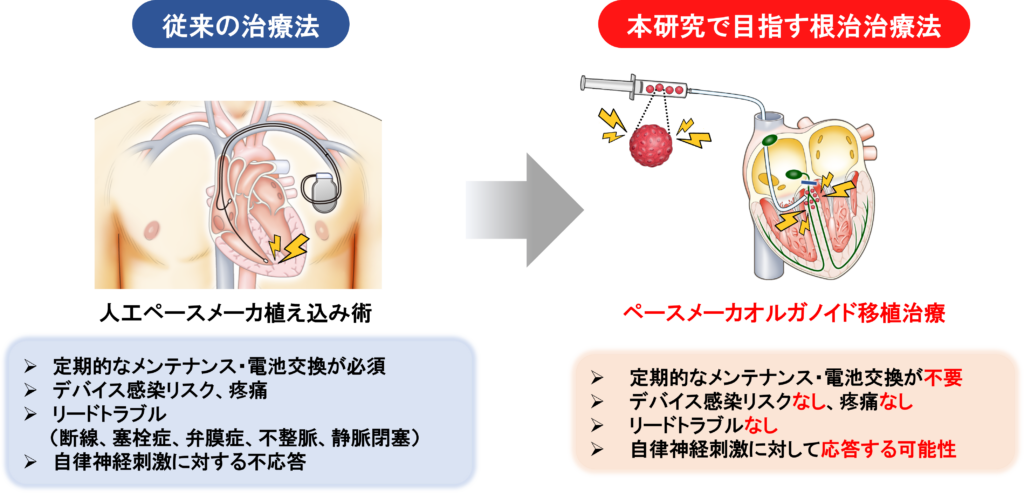
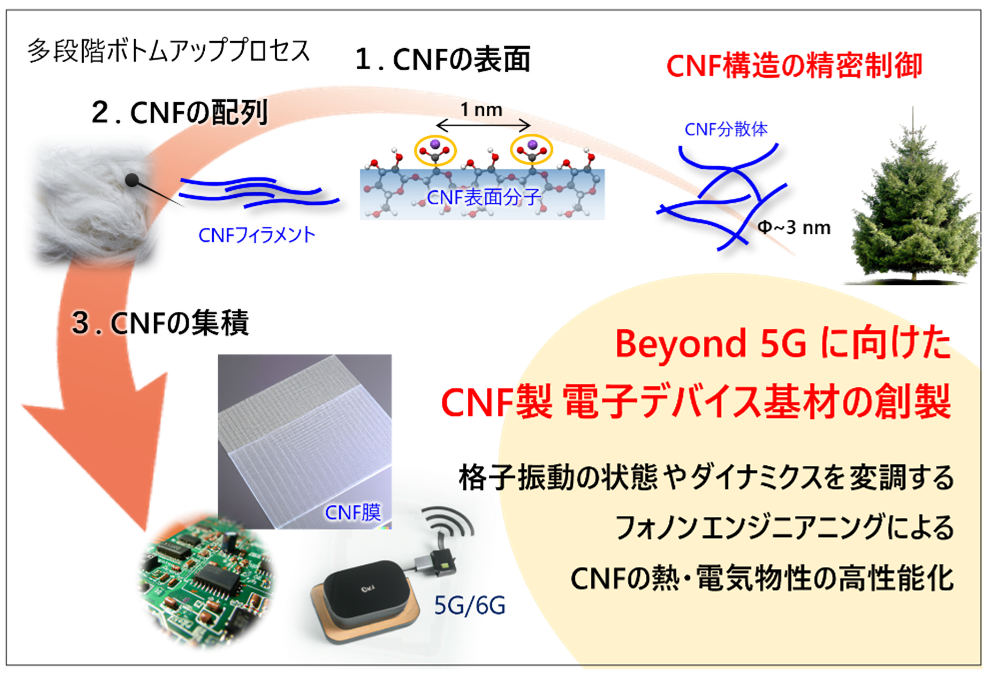
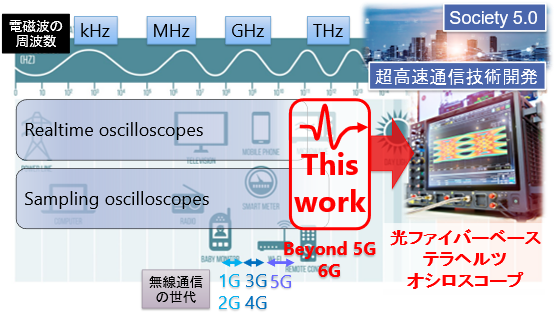
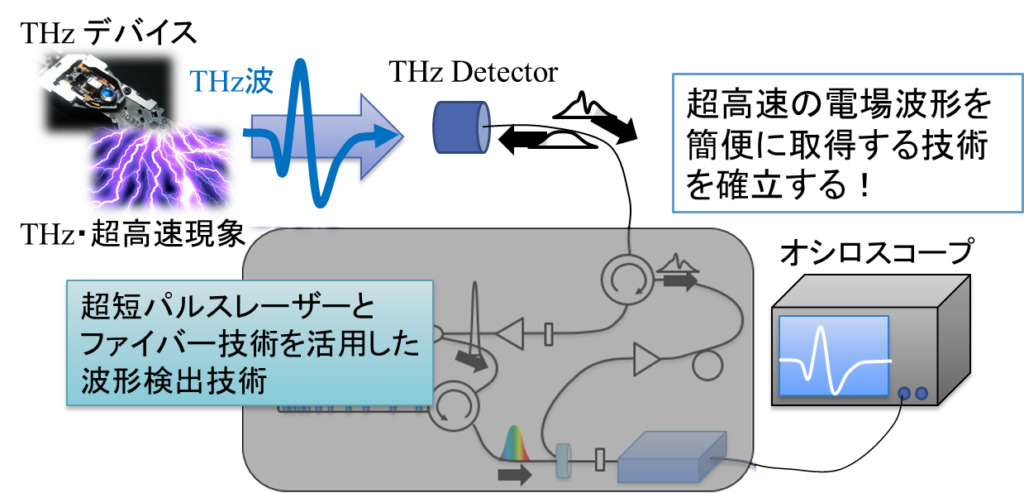
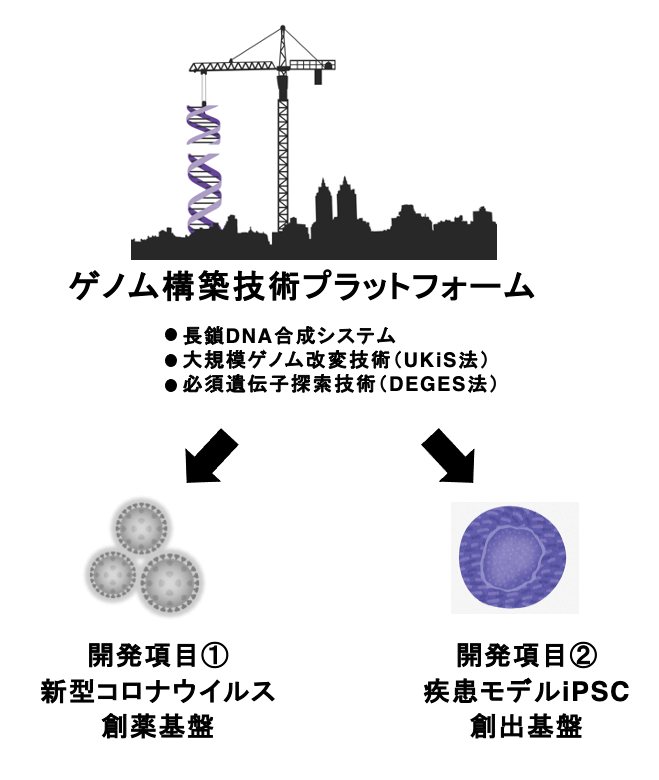
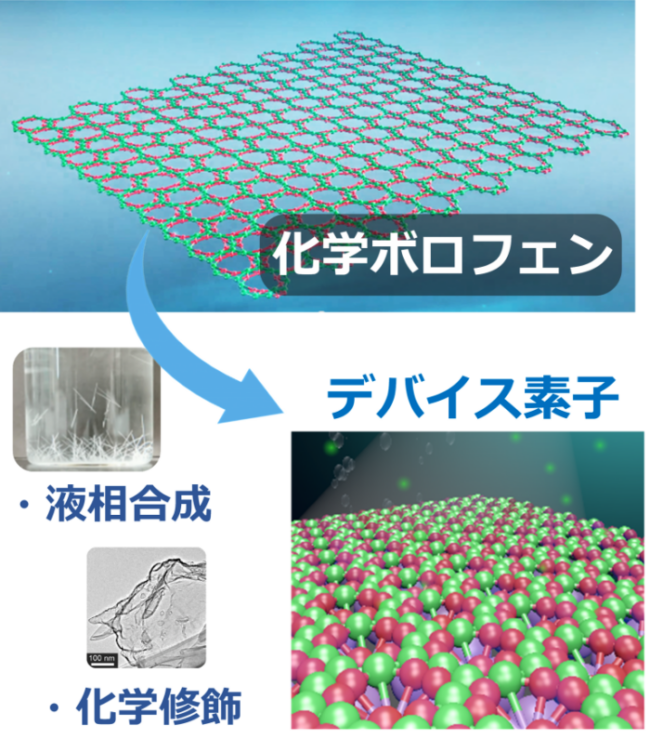
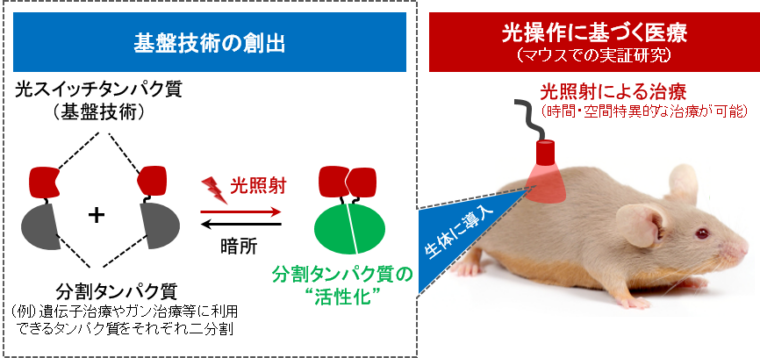
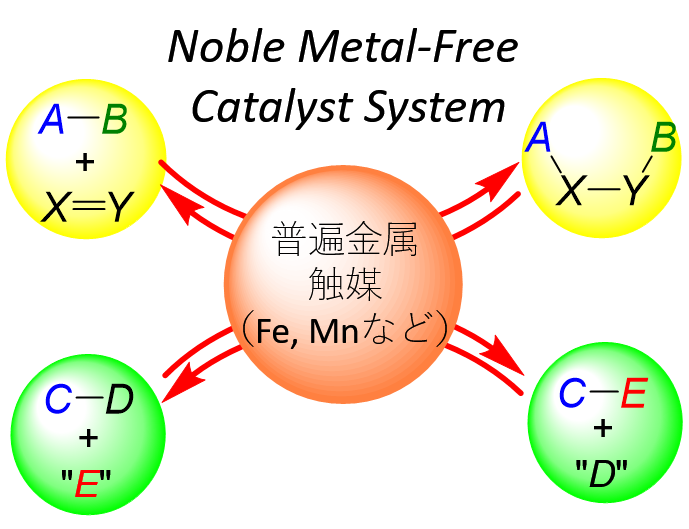
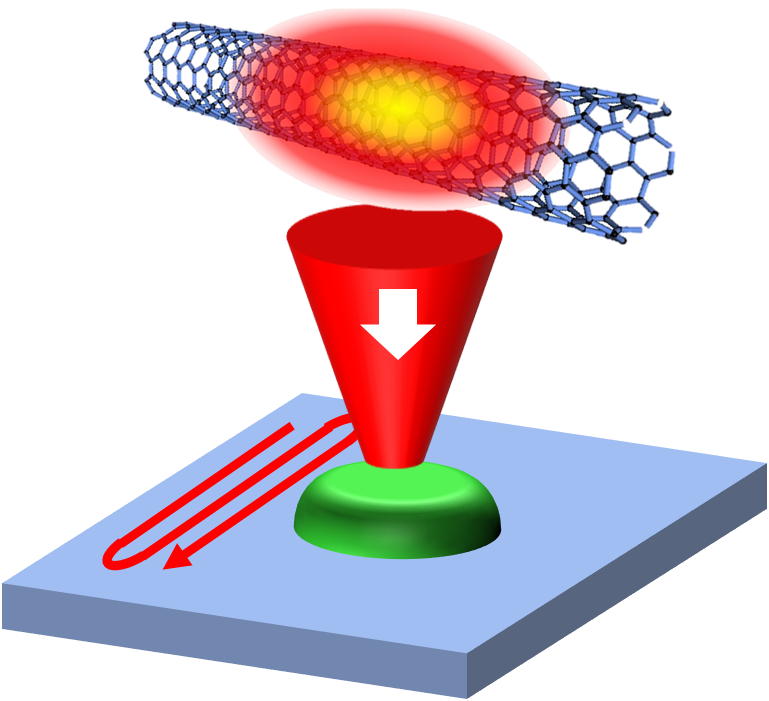
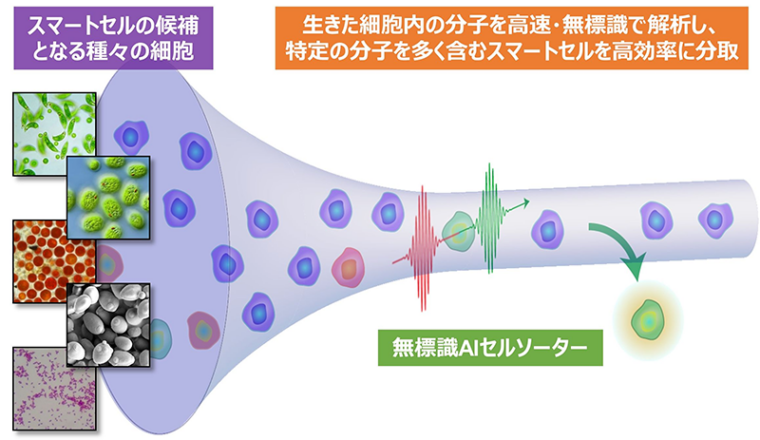
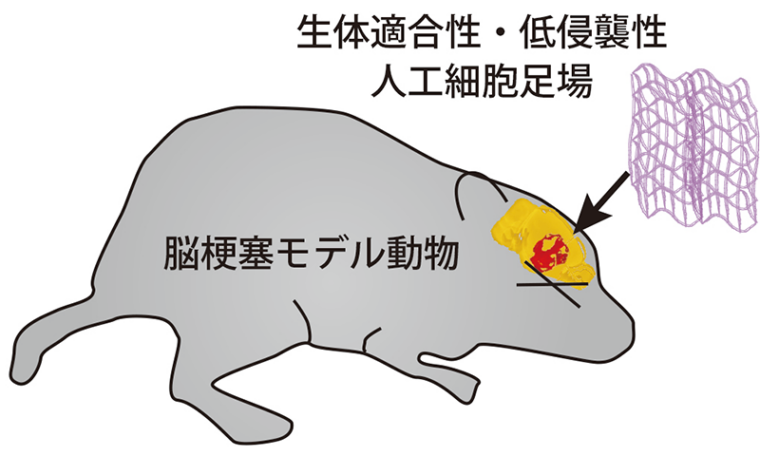
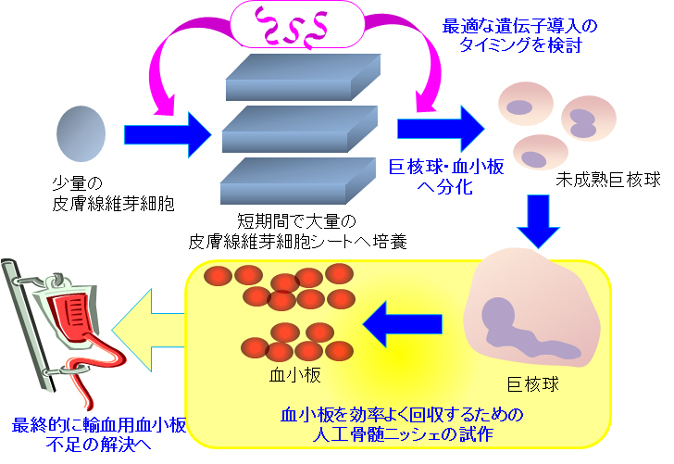
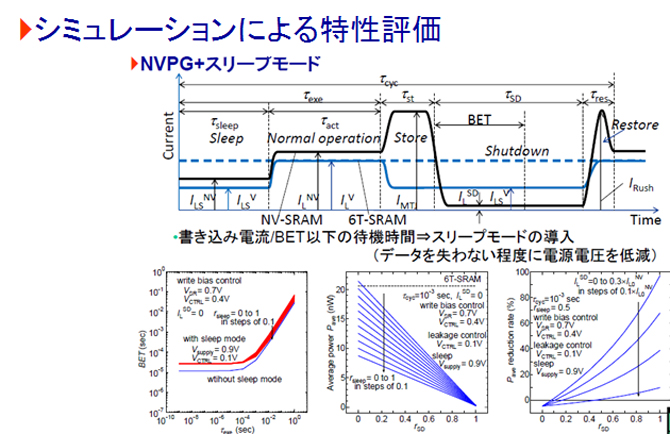
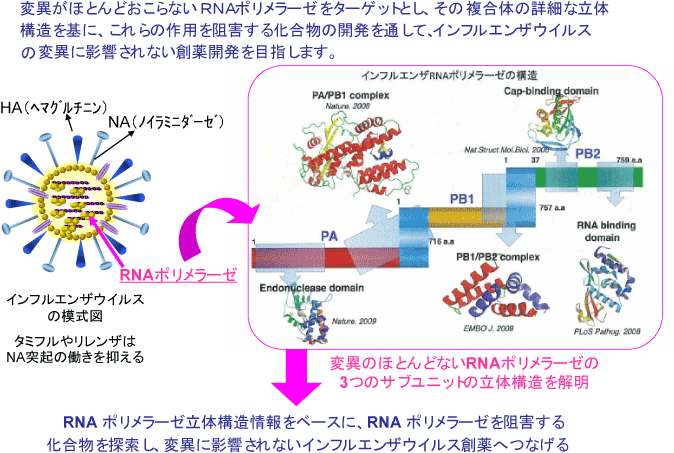
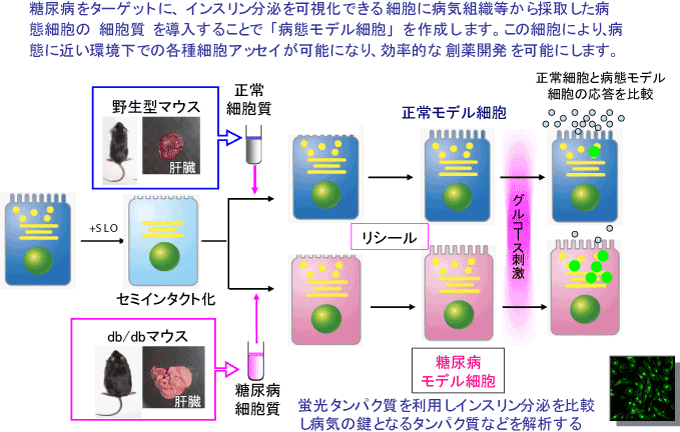
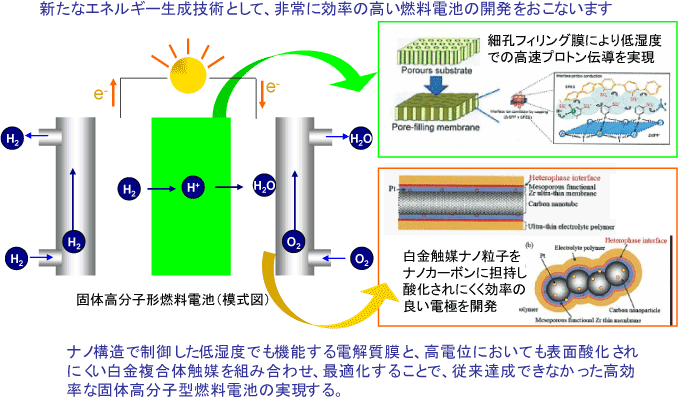
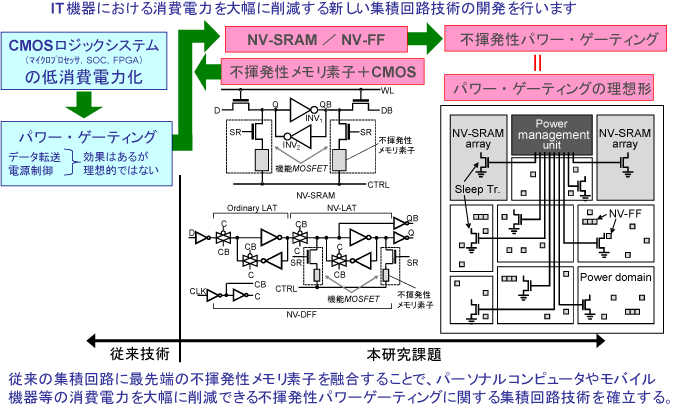
KISTECが主要研究分野として掲げる「基礎科学・計測」、「ナノテクノロジー・材料科学」、「エレクトロニクス・情報・通信」、「ライフサイエンス」のいずれか、またはこれらの分野を超えた複合領域に属するものであって、本事業の事業目的に合致する研究課題を広く募集します。
事業体制
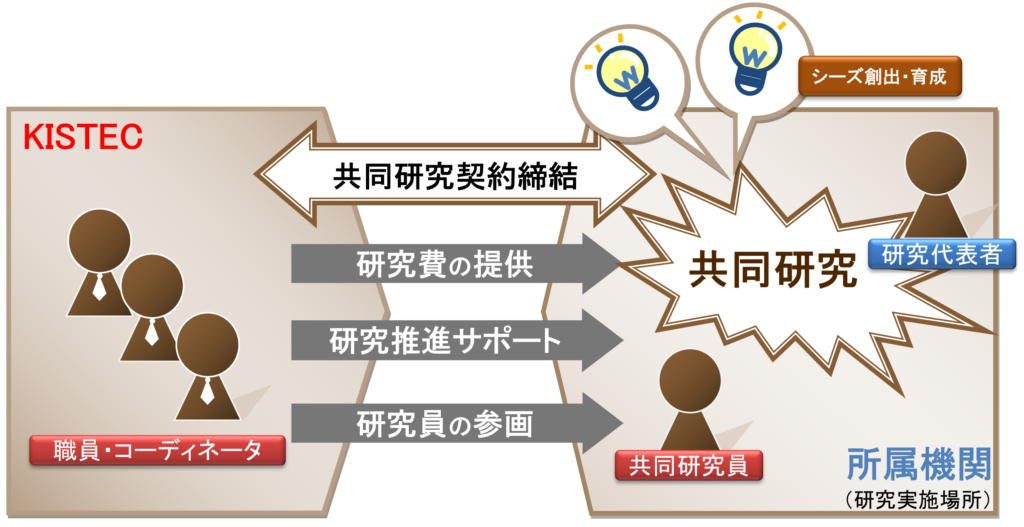
採択された研究課題の提案者が自ら研究代表者となって、KISTECと研究代表者の所属機関との間で共同研究契約を締結し、所属機関を研究実施場所として本事業を実施していただきます。KISTECは、研究課題毎に専任の研究員またはKISTEC技術部に所属する研究員を共同研究員として研究業務に参画させます。当該共同研究員の専任に際し、研究代表者はKISTECに対して相応しい研究者を推薦することができます。また、共同研究を実施するうえで、KISTECの職員らによる様々な支援を受けることができます。
他事業への展開
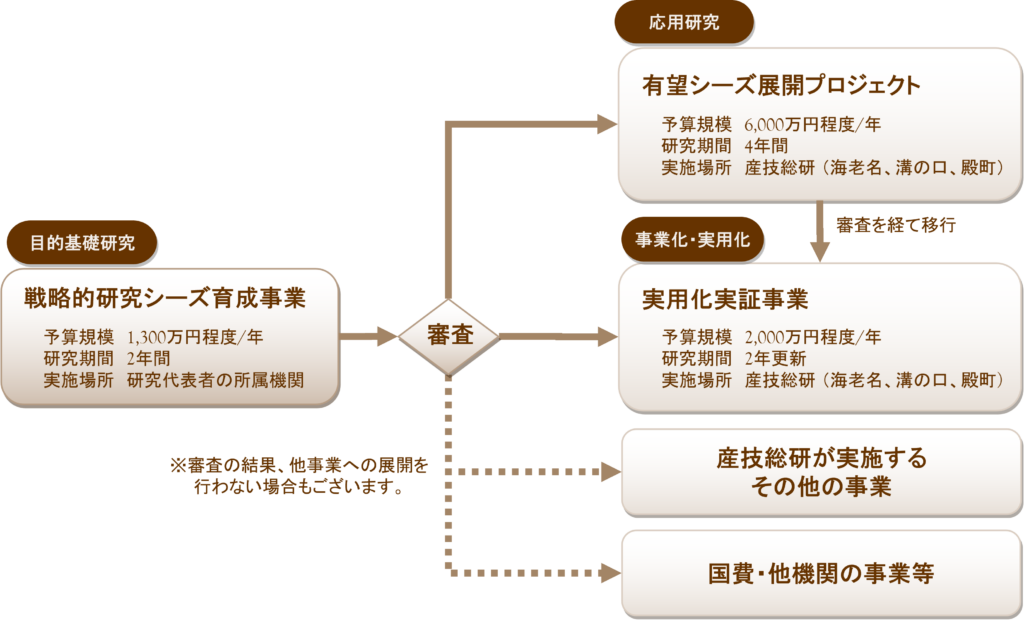
本事業終了後、研究の進捗や成果等に応じて、審査を経て他の研究事業へ展開(ステップアップ)します。審査の結果、他事業へ移行せず終了する場合があります。また、産技総研が実施する他の事業、国や他機関の研究事業等への展開を提案させていただく場合があります。
公募について
公募情報はホームページ上で公開します。詳細は「募集要項」タブをご参照ください。
お問い合わせ
以下のEメールアドレスへご連絡ください。
rep-kenkyu★kistec.jp(アドレス内の「★」を「@」に変更してご利用ください)
採択者の所属・役職は、採択時のものとなっております。
令和8年度公募 概要 ※令和8年度応募受付は終了しました。
| 募集課題 | 「基礎科学・計測」、「ナノテクノロジー・材料科学」、「エレクトロニクス・情報・通信」、「ライフサイエンス」のいずれか、またはこれらの分野を超えた複合領域に属する研究課題 |
| 研究期間 | 令和8年4月1日 ~ 令和10年3月31日 (2年間) |
| 事業予算 | 1テーマ 年間1,300万円程度 (人件費等を含む) |
| 応募受付期間 | 令和7年9月16日(火) ~ 9月25日(木) |
| 応募方法 | 下記の事前登録フォームから事前登録を行ってください。折り返し提案書提出用のメールアドレスを通知します。応募期日までに指定アドレス宛に研究提案書と主要論文等(別刷)を添付し、ご提出ください。 |
| 選考 | 一次選考(書面審査) 二次選考(面談審査)令和7年12月8日(月)、令和7年12月9日(火) |
| 採否通知 | 令和8年1月頃に電子メールにて通知 |
令和8年度公募 要項・様式等ダウンロード
募集要項
1.戦略的研究シーズ育成事業の推進
(1)共同研究
・KISTEC と所属機関との間で共同研究契約を締結します。応募にあたって、本要項の内容を理解したうえで本事業の実施可否について予め所属機関へ確認してください。
・採択後、提案者は研究代表者として、所属機関の身分のままKISTEC の共同研究員とともに共同研究を推進していただきます。
(2)共同研究実施場所
・共同研究の実施場所は研究代表者の所属機関とします。本事業が所属機関とKISTEC とが連携しながら新たなステージを目指すものであることに鑑みて、共同研究実施場所は神奈川県内またはその近郊に確保してください。
(3)KISTEC研究員の参画(共同研究員)
研究代表者は、共同研究の実施にあたって、次のいずれか、または併用によるKISTEC 研究員の参画方法を決定します。
A.専任研究員の参画
・研究代表者が推薦する博士号取得者をKISTEC の規定に基づいて新規に雇用し、専任の研究員として共同研究へ参画させます。(推薦者がいない場合は公募となります。)
・専任研究員の給与・手当および社会保険料等は本事業予算から支出します。
・専任研究員は共同研究実施場所にて研究に従事し、研究代表者の所属機関は専任研究員を受け入
れていただきます。
B.技術部研究員の参画
・KISTEC 技術部(機械・材料技術部、電子技術部、情報・生産技術部、化学技術部または川崎技術支援部)の研究員が、設定したエフォートの範囲で共同研究に参画します。
・研究活動を支援するため、研究課題毎にKISTEC職員を担当者として配置します。
・KISTEC職員は、担当した採択課題を研究プロジェクト等にステップアップさせるために、進捗状況等を把握します。
(4)KISTECによる支援等
・研究活動を支援するため、採択課題毎にKISTEC 職員を担当者として配置します。
・担当職員は、研究推進のために進捗状況等を把握し、共同研究に係る知的財産権の取り扱い、外部連携に伴う契約、予算執行に関する事務を行います。
・科学技術コーディネーター、研究推進統括監、技術推進統括監等が本事業の目的達成に向けた助言やサポートを行います。
(5)知的財産権の帰属
・研究活動により得られた発明等の知的財産権については、原則的に、研究代表者、専任研究員及びその他の発明等をなした者による寄与の割合に応じて所属機関がそれぞれ承継し、持分等の詳細については所属機関とKISTECとの間の共同研究契約に基づいて取り扱うこととします。
・本事業によって得られた知的財産権等に基づいてKISTEC研究事業にステップアップした場合は、当該知的財産権がその後の研究活動、技術移転活動等に支障が生じることがないよう調整させていただく場合があります。
(6)KISTEC 研究事業へのステージゲート審査
・採択課題をKISTEC 研究事業等へステップアップさせるか否かの判断を行うため、研究代表者は本事業の二年度目にKISTEC 研究事業の提案書を新たに作成し、対面プレゼン形式でステージゲート審査を行います。審査の結果、ステップアップすることなく研究を終了とさせていただくことがあります。
2.提案者の要件
研究代表者となる方ご本人から提案していただきます。提案者の要件は次のとおりです。
・自ら研究構想の発案者であるとともに、その構想を実現するためのリーダーシップを持って研究を推進する意思のある方。
・本事業及びKISTEC 研究事業等を通じて、研究全体に責任を負える方。
・共同研究開始時点で50歳以下の方。
※ステップアップ等により研究事業が長期に渡る可能性があるため一定の年齢制限を設けています。
3.対象となる研究課題
(1)研究の位置付け:目的基礎研究
※ 目的基礎研究とは、イノベーション創出が期待できるシーズ創出直後若しくは創出間近の研究段階を示します。
(2)研究課題:下記研究分野のいずれか、またはこれらの複合領域に属する研究課題
「基礎科学・計測」
「ナノテクノロジー・材料科学」
「エレクトロニクス・情報・通信」
「ライフサイエンス」
(4)第二期中期計画:
KISTECは神奈川県知事から指示を受けた第二期(令和4年度~令和8年度)の中期目標を達成するための計画(第二期中期計画)に基づいて研究活動を行っています。
4.研究期間
原則2 年間(令和8年4 月1 日から令和10年3 月末まで)
※KISTEC と所属機関との間で、年度毎に共同研究契約を締結します。
5.研究費
(1)基準単価
一課題あたりの事業予算:1,300 万円程度/年 (専任研究員の人件費及び間接経費を含む)
(2)研究費の使途
本事業における研究課題の推進に直接必要な経費に支出できます。執行ルールについては所属機関の規程を適用していただきます
(3)共同研究費の支払い
・共同研究費は、本事業予算からKISTEC が直接執行する経費(専任研究員の人件費、その他諸経費)を差し引いて、所属機関が発行する請求書に基づいて概算払いします。
・所属機関において共同研究員の受け入れのための費用(共同研究料等)が生じる場合には、本事業予算から支払います。
(4)経費の支払い
・共同研究費は単年度会計(会計期間:4月~3月)で集計し、共同研究契約で定められた期日までに所定の様式にて経理報告書を提出していただきます。なお、共同研究費の年度繰り越しは認められません。
6.選考
(1)選考スケジュール
応募締め切り後、一次選考(書類審査)、二次選考(面接審査)を経て令和8年1月頃に採択内定の予定です。
二次選考(面談審査)は以下のいずれかの日程で行います。予めスケジュールの調整を行ってください。
二次選考実施日 令和7年12月8日(月)、令和7年12月9日(火)
(2)選考の視点
独創性 :提案者自身の着想であること
地域への貢献:地域の経済的価値の創出や地域の社会的価値の創出が期待できること
実現性 :提案された研究構想を実現するための手がかりが得られていること
(3)応募寳方法
・本事業は公募制です。提案者は指定様式の「研究提案書」に主要論文の別刷り等(5件以内)を添付し、受付期間中に応募フォームにて登録のうえ指定先メールアドレスへご提出ください。
・本事業への応募は提案者1名につき1課題までとします。また、複数名による連名での提案は認められません。
・本事業は、KISTEC 研究事業等へつながる研究シーズの育成を目的としているため、ステップアップした場合の研究期間4 年間を含め、計6 年間の研究計画を作成していただきます。
・研究提案書の記入内容に不明な点がある場合及び書類に不備がある場合には、KISTEC 事務局より提案者に説明を求め、書類の修正や再提出を求める場合があります。この場合において、修正や再提出が指定した期日に間に合わない場合は辞退したものとみなします。
・研究提案書及びその他の提出書類は本事業の審査のために使用し、提案者の利益の維持、個人情報保護及びその他の観点から応募内容に関する秘密は厳守します。なお、研究提案書およびその他の提出書類は返却しません。
(4)採択件数
3件程度(予定)
その他詳細は募集要項(PDF)をご参照下さい。